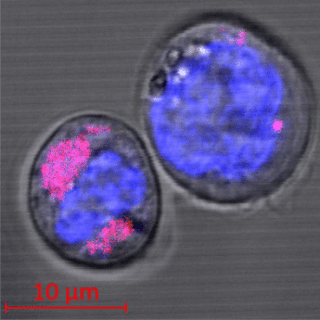
Углеродные наночастицы служат потенциальным инструментом в биомедицинских применениях. Например, они используются для адресной доставки биологически активных соединений в клетки организма.
В настоящее время исследовательская группа из отделов физики, медицины и химии Университета им. Генриха Гейне в Дюссельдорфе (HHU) изучила природу этих частиц, чтобы определить, являются ли они потенциально вредными для организмов и как клетки способны бороться с ними после они были интегрированы. Результаты междисциплинарного исследования были недавно опубликованы в журнале Scientific Reports .
Размер наночастиц меньше 5 нм, нанометр равен одной миллионной миллиметра, что примерно равно размеру макромолекул. Такие мелкие частицы легко поглощаются клетками организма.
Эта функция имеет два аспекта. Во-первых, наночастицы превращаются в превосходные средства для целенаправленной доставки широкого спектра веществ или соединений (прикрепленных к наночастицам) в нормальные и больные клетки.
Однако наночастицы могут также представлять риск для здоровья, например, в отношении твердых частиц. Процессы сгорания являются одним из методов, при котором образуются твердые частицы, и некоторые из них можно отнести к категории наночастиц.
Эти частицы достаточно малы, чтобы пересечь гематоэнцефалический барьер и проникнуть в организм: легкие содержат слизистую оболочку бронхов, которая не отфильтровывает частицы, что позволяет им проникать в легочные альвеолы и в конечном итоге попадает в кровоток .
В сотрудничестве с рабочими группами из отдела химии ученые HHU из отдела гематологии, онкологии и клинической иммунологии, работающие под руководством профессора доктора Райнера Хааса и из Института экспериментальной физики конденсированных сред, работающего под руководством профессора доктора Томаса Хайнцеля, обнаружили что именно происходит, когда такие наночастицы поглощаются клетками организма.
Ученые использовали наночастицы, изготовленные из графена – уникальной формы углерода, содержащей двумерные (2D) слои гексагональных углеродных колец. Впоследствии они добавили эти наночастицы на основе графена в уникальные гемопоэтические стволовые клетки, известные как стволовые клетки CD34 + .
Эти типы клеток имеют тенденцию делиться на протяжении всей своей жизни, и, следовательно, они особенно чувствительны к разрушительным воздействиям окружающей среды. Считается, что по сравнению с другими и более устойчивыми типами клеток стволовые клетки с большей вероятностью будут повреждены наночастицами.
Междисциплинарная группа ученых, расположенная в Дюссельдорфе, продемонстрировала, что эти углеродные наночастицы попадают в клетки, где они заключены в лизосомы, которые представляют собой специальные органеллы. Эти лизосомы действуют как своеобразная единица удаления отходов для организма, где инородные тела накапливаются и обычно распадаются с помощью ферментов. И наоборот, следователи не обнаружили такого процесса в течение периода экспериментов, который продолжался в течение многих дней.
Когда исследователи сравнили активные гены стволовых клеток («экспрессия генов») с включением и отсутствием наночастиц, они наблюдали изменения только в одном из 20 800 зарегистрированных выражений; незначительные эффекты были измерены в дополнительных 1171 экспрессии генов.
Инкапсуляция наночастиц в лизосомах гарантирует, что эти частицы надежно хранятся, по крайней мере, в течение нескольких дней – на протяжении наших экспериментов – и не могут повредить клетку. Это означает, что клетка остается жизнеспособной без каких-либо существенных изменений в экспрессии генов .
Доктор Томас Хайнцель, профессор, Институт экспериментальной физики конденсированных сред, HHU
Это восприятие является значительным, если наночастицы необходимо использовать для транспортировки лекарств в клетку. Тем не менее, экспериментальная структура, используемая в этом случае, не позволяет делать какие-либо долгосрочные заявления в отношении увеличения вероятности клеточных мутаций, ведущих к раку.
Исследование проводилось в тесной взаимосвязи между факультетом математики и естественных наук HHU, медицинским факультетом и университетской клиникой Дюссельдорфа. Докторская стипендия первого автора Стефана Фасбендера была профинансирована Дюссельдорфской школой онкологии (под руководством профессора доктора Себастьяна Вессельборг).
Близость больницы и университета и их тесные связи с точки зрения содержания обеспечивают HHU особенно плодотворную среду для трансляционных исследований, где понимание и опыт фундаментальных исследований сочетаются с аспектами, относящимися к лечению .
Доктор Райнер Хаас, профессор кафедры гематологии, онкологии и клинической иммунологии, HHU
Источник: https://www.uni-duesseldorf.de/
 Диэнай
Диэнай