Исследуя медицину Джона Хопкинса, просматривая полные генетические последовательности человека с рубцовой болезнью легких и 13 его родственников, они обнаружили ошибку кодирования в одном гене, который, вероятно, ответственен за редкую форму болезнь и аномально короткие защитные ДНК-шапки на хромосомах, долго ассоциировавшиеся с ней.
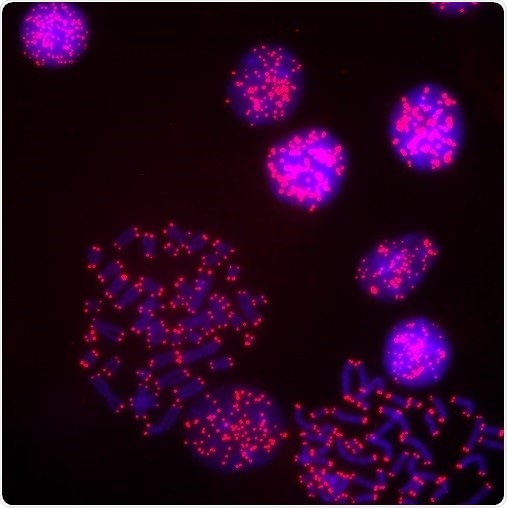
Изображение человеческих теломер в клетках. Каждая теломер показана красными точками в покоящихся ядрах клеток (кружки) и клеток, которые делятся (разделенные линейные хромосомы). Предоставлено: Мэри Арманиос
.
Ошибка была обнаружена в последовательности ДНК гена ZCCHC8, и она уменьшает вдвое выработку белка, необходимого для поддержания этих колпачков – так называемых теломер – на критической длине, утверждают исследователи. Это открытие, добавляет они, означает, что недостаток, вероятно, станет частью небольшого, но растущего списка диагностических маркеров для так называемых синдромов коротких теломер.
Отчет о работе, посвященной заболеванию, известному как идиопатический легочный фиброз (IPF), был опубликован онлайн 5 сентября в журнале Genes & Development .
Сочетание клинического и молекулярного подходов может быть очень эффективным в попытках понять причину генетического заболевания и его биологию. Мы обнаруживаем, что существует много генных путей, которые могут нарушать регуляцию длины теломер. За последние 15 лет Арманиос выявил пять из семи связанных с теломерами генетических ошибок в семьях с фиброзом легких. Теперь есть восьмое. "
Мэри Арманиос, доктор медицинских наук, профессор онкологии в онкологическом центре им. Джона Хопкинса Киммеля и клинический директор Центра теломеров при Джонсе Хопкинсе
IPF встречается примерно в 100 000 человек в США, говорит Арманиос, и создает рубцы легких, не связанные с курением или другими факторами окружающей среды. Предполагается, что примерно каждый пятый человек с IPF имеет наследственную форму заболевания, и половина из этих случаев связана с унаследованной тенденцией к очень коротким теломерам.
Теломеры защищают концы хромосомной ДНК, как пластиковые трубки на концах шнурков, и они обычно укорачиваются при старении. Состоящие из повторяющихся последовательностей ДНК нормальные теломеры имеют достаточную длину, чтобы противостоять эрозии, которая происходит в течение нормальной продолжительности жизни. Однако некоторые люди рождаются с аномально короткими теломерами, что вызывает проблемы со способностью клеток делиться и размножаться и приводит к целому ряду расстройств, включая IPF, недостаточность костного мозга, некоторые формы заболеваний печени и рак костного мозга, называемый миелодиспластическим. синдромов.
В предыдущих исследованиях Арманиос показал, что для правильного выбора терапии важно знать, имеет ли человек с IPF короткие теломеры. Если речь идет о коротких теломерах, лечение некоторых расстройств должно включать в себя снижение доз химиотерапии до трансплантации костного мозга, меньшее использование иммунодепрессантов и использование доноров легкого и костного мозга, у которых нет связанных с теломерами генетических ошибок.
Генные ошибки, которые происходят в семьях с IPF, обычно редки среди населения, поэтому их трудно точно определить, говорит Арманиос. «Это все равно, что искать иголку в стоге сена», – говорит она. Таким образом, исследователи должны разбить стог сена на части и изучить генетику отдельных семей, чтобы найти наследственных преступников.
Чтобы найти восьмую мутацию, они выполнили секвенирование всего генома, чтобы исследовать последовательности ДНК пациента с IPF и 13 его родственников. Во-первых, они обнаружили, что у некоторых членов семьи низкий уровень компонента РНК теломеразы, или TR. Это один из двух биохимических фрагментов теломеразы, фермента, который удлиняет теломеры. С меньшим количеством TR меньше теломеразы доступно для поддержания, восстановления и ремонта концевых колпачков ДНК.
Затем, исследователи сравнили различия между всем геномом между членами семьи с низким уровнем TR и с нормальными уровнями. Среди измененных участков ДНК в членах семьи с низким уровнем TR, Арманиос и ее команда сузили свой поиск до участка ДНК на хромосоме 12, длина которого составляет 17 миллионов пар оснований (из 3 миллиардов пар оснований в геноме человека). В этой области ранее не было известно, что ген ZCCHC8 выполняет функции, связанные с поддержанием теломер.
Однако, Арманиос и ее команда измерили белок, полученный из содержащего ошибку гена ZCCHC8, и обнаружили, что у членов семьи с низким уровнем TR было половину количества белка ZCCHC8 по сравнению с членами семьи, у которых были нормальные количества TR.
Чтобы определить функцию белка ZCCHC8, команда Арманиоса использовала технологию редактирования генов CRISPR в клетках и мышах человека, чтобы обнаружить, что белок обычно обрезает концы хвоста TR, чтобы они могли созревать и функционировать как часть теломеразы. Но клетки и мыши, лишенные ZCCHC8, имеют дополнительное количество не усеченных TR, что приводит к более короткой версии молекулы, которая больше не может становиться частью теломеразы.
Арманиос говорит, что результаты могут потенциально раскрыть способ разработки методов лечения, которые восстанавливают баланс TR в клетках, чтобы помочь с функцией теломеразы.
В настоящее время врачи, которые подозревают, что у человека синдром короткой теломер, могут пройти длину теломер и провести генетическое тестирование, которое включает семь ранее выявленных генных ошибок. Арманиос говорит, что ошибка гена ZCCHC8 будет добавлена в диагностический генный тест.
Мы перешли от знания лишь нескольких генетических ошибок, связанных с небольшим процентом случаев IPF десять лет назад, к пониманию того, что способствует более чем трети семей, чей ген IPF не был охарактеризован, и почти 10% других Дела IPF. "
Мэри Арманиос, М.Д.
Исследование финансировалось Национальным институтом рака Национального института здравоохранения (RO1CA225027, P30CA006973), Национальным институтом сердца, легких и крови (RO1HL119476, T32HL007534, F32HL142207) и Национальным институтом общих медицинских наук (T32GM007309); программа Фонда реституции сигарет Мэриленда, Фонд Содружества; Фонд Гари Уильямса; S & R Foundation Kuno Award; Фонд Ученых Турок; Национальный научный фонд и П. Годрей.
В состав исследовательской группы входили Дастин Л. Гейбл, Валерия Гайсинская, Кристина Атик, Коновер Талбот-младший, Бюнгхак Канг, Сьюзен Стэнли, Элизабет Пью, Нурия Амат-Кодина, Кара Шенк, Кори Брайтон и Лилиана Флореа из Джонс. Хопкинс и Мурат Аркасой из Медицинского факультета Университета Дьюка.
 Диэнай
Диэнай