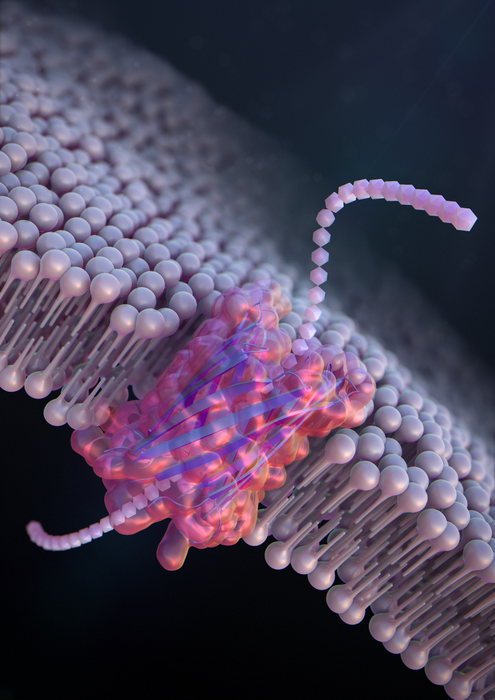
Ученые в Японии впервые создали пептиды, созданные снизу вверх, содержащие цепочки аминокислот, которые могут образовывать синтетические нанопоры для идентификации и облегчения сортировки отдельных молекул генетического материала в липидной мембране.
Биологические нанопоры – это большие каналы, состоящие из порообразующих белков, которые могут идентифицировать определенные молекулы, но такие естественные каналы трудно идентифицировать, что ограничивает предлагаемые применения в экономичном быстром секвенировании ДНК, обнаружении малых молекул и т. Д.
Зондирование нанопор – это мощный инструмент для безметочного обнаружения одиночных молекул. Это первый раз, когда ДНК и полипептиды были обнаружены с помощью нанопоры, созданной de novo.
Рюдзи Кавано, автор исследования, профессор Токийского сельскохозяйственного и технологического университета
Их результаты были опубликованы в выпуске журнала Nature Nanotechnology от 22 ноября и
.
Новоинженерные нанопоры конструируются «с нуля», согласно Кавано, и обладают перспективой имитации природных белков и их способностью обнаруживать определенные белки.
Примечательно, что, по словам Кавано, они также могут быть сконструированы в качестве искусственных молекулярных машин, которые могут обнаруживать гораздо более широкий спектр молекул, что может помочь прояснить связь между структурой и функцией в целевых белках.
Кавано отметил, что все белки обладают новой структурой и размером.
Сложенная структура белков определяется их линейной полипептидной последовательностью и дает начало специфической функциональности белка. Уникальная первичная структура является результатом структурной эволюции, такой как мутации и отбор аминокислотных остатков с течением времени. Выявление взаимосвязи между этой первичной информацией и структурой белка – одна из конечных целей науки.
Рюдзи Кавано, автор исследования, профессор Токийского сельскохозяйственного и технологического университета
Чтобы сформировать большие искусственные нанопоры, которые могут точно обнаруживать и распознавать молекулы для практического применения, Кавано и его команда создали пептид под названием SV28. С двумя плечами аминокислот, скрученными под острым углом, и точными зарядами на концах, выравнивание пептида в форме шпильки можно точно регулировать путем приложения напряжения.
Пептид может ориентироваться с образованием нанопористых структур размером от 1,7 до 6,3 нм, идеально подходящих для восприятия молекул ДНК.
Ученые также изменили SV28, интегрировав мутацию, которая заставляет структуру пептида изгибаться и скручиваться определенным образом. В полученном пептиде образовались равномерно диспергированные поры размером 1,7 нм каждая, способные идентифицировать одну полипептидную цепь или половину белка.
Это достижение может быть использовано для облегчения понимания связи между структурой и функцией белка.
На последующих этапах команда стремится разработать различные пептиды и белки для создания различных типов нанопор для поддержки секвенирования пептидов, работы в качестве молекулярных роботов и т. Д.
Другими участниками исследования являются Кейсуке Симидзу, Масатака Усами и Икуро Мидзогути, факультет биотехнологии и наук о жизни Токийского университета сельского хозяйства и технологий; Батсайхан Миджиддорж и Изуру Кавамура, Высшая школа инженерии, Йокогамский национальный университет; Шухей Ёсида, Сиори Акаяма, Ёсио Хамада и Кендзи Усуи, факультет передовых инновационных исследований в области науки и технологий, Университет Конан; и Акифуми Охьяма из Высшей школы инженерных наук Йокогамского национального университета
Кавамура также является членом Высшей школы инженерных наук Йокогамского национального университета. Миджиддорж также является членом Школы инженерных и прикладных наук Национального университета Монголии.
Это исследование было поддержано Японским обществом содействия науке (19H05382 и 21H00390), Министерством образования, культуры, спорта, науки и технологий (19H00901) и Монголо-японской программой развития инженерного образования частично.
Ссылка на журнал:
Симидзу К., и др. . (2021) Разработка de novo нанопоры для обнаружения одиночных молекул, которая включает в себя β-шпилечный пептид. Природа Нанотехнологии . doi.org/10.1038/s41565-021-01008-w.
Источник: https://www.tuat.ac.jp/en/[19459007visible
 Диэнай
Диэнай