Гетерогенность самих раковых клеток является одной из основных трудностей, с которыми приходится сталкиваться при разработке эффективных и целевых методов лечения рака. Из-за этого изменения иммунной системе становится сложно идентифицировать опухоли, реагировать на них и активно бороться с ними .
Но новые достижения в области нанотехнологий в настоящее время делают возможным создание целевых и персонализированных «вакцин» для лечения рака.
Новое исследование, опубликованное недавно в журнале Science Advances описывает использование заряженных наноразмерных металлоорганических каркасов и рентгеновских лучей для образования свободных радикалов внутри опухолевой ткани для непосредственного уничтожения раковых клеток.
Более того, можно использовать те же каркасы для создания иммунных сигнальных молекул, называемых PAMP, для запуска иммунного ответа против опухолевых клеток. Объединяя эти два метода в одну «вакцину», которую можно легко вводить, эта новая технология может проложить путь к улучшению местного и системного лечения трудноизлечимых видов рака.
В рамках сотрудничества между Lin Group из химического факультета Чикагского университета и лабораторией Вайксельбаума Медицинского университета Чикаго исследователи объединили опыт биологии рака и неорганической химии для решения сложной проблемы правильного нацеливание и запуск врожденного иммунного ответа против рака.
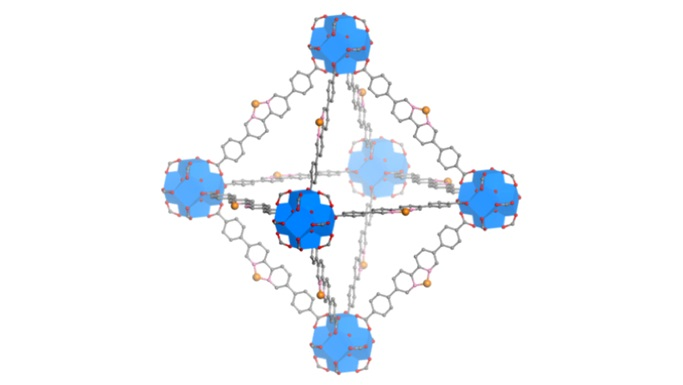
В этом исследовании использовались особые свойства наноразмерных металлоорганических каркасов (nMOF), которые представляют собой наноразмерные структуры, состоящие из повторяющихся элементов, расположенных в виде решетки и способных проникать в опухоли.
Такие nMOF можно облучать с помощью рентгеновских лучей для получения высоких концентраций свободных кислородных радикалов, тем самым напрямую убивая раковые клетки и генерируя воспалительные молекулы и антигены, помогающие иммунной системе идентифицировать и очищать раковые клетки, что очень похоже на вакцина.
Более того, решетчатая структура nMOF делает их идеальными переносчиками для прямой доставки противораковых лекарств в опухоли. Но до настоящего времени было сложно вызвать врожденный и адаптивный иммунный ответ, необходимый для уничтожения раковых опухолей.
В рамках нового исследования команда дополнительно усовершенствовала свою технику. Они создали новый вид структуры nMOF, которая может быть загружена лекарствами, называемыми патоген-ассоциированными молекулярными структурами (PAMP).
При применении nMOF к раковым опухолям облучение ткани оказало двойное воздействие: оно активировало nMOF, чтобы разрушить местные раковые клетки, чтобы создать антигены против опухоли, и высвободило PAMP, что впоследствии вызвало гораздо более мощную активацию иммунный ответ на опухолевые антигены.
Этот удар «один-два» может уничтожить раковые клетки как поджелудочной железы, так и толстой кишки с высокой эффективностью, даже в моделях опухолей, которые значительно устойчивы к другим типам иммунотерапии.
Исследователи провели дополнительные эксперименты на мышах и обнаружили, что они могут расширить воздействие nMOF даже на отдаленные опухоли, применяя ингибиторы контрольных точек, что дает новые надежды на лечение рака как системного, так и местного действия с помощью этого метода.
Включив доставку PAMP с nMOF мы впервые смогли действительно усилить иммунный ответ на антигены . Это полностью отличается от всех наших предыдущих исследований, поскольку мы показали, что nMOF плюс PAMP могут влиять на все аспекты, необходимые для активации иммунной системы .
Вэньбинь Линь, доктор философии, старший автор исследования, и профессор химии Джеймс Франк, Медицинский центр Чикагского университета
« Мы можем использовать эту наноформулировку для обеспечения персонализированной вакцинации против рака, которая будет работать для любого пациента, потому что эта стратегия не будет зависеть от неоднородности, которую мы наблюдаем среди разных пациентов », – добавил Лин.
Воздействие лечения было настолько значительным, что ученые стремятся довести технологию до клинических испытаний, в то время как другие версии технологии nMOF уже проходят испытания с обнадеживающими результатами до сих пор.
У этой системы двоякое великолепие . Во-первых, он может улучшить локальный контроль опухолей за счет увеличения убивающей силы рентгеновских лучей. Во-вторых, хотя и проявлялся интерес к использованию излучения для стимуляции иммунного ответа для борьбы с раком, оказалось, что это сложнее, чем мы думали .
Ральф Вайксельбаум, доктор медицины, соавтор исследования и Даниэль К. Людвиг, заслуженный профессор радиационной и клеточной онкологии, Медицинский центр Чикагского университета
« В этом случае nMOF способны активировать врожденную и адаптивную иммунные системы, что делает эту технологию очень перспективной для лечения рака в клинике », – добавил Вайксельбаум, который также является председателем Отделение радиационной и клеточной онкологии в Чикаго.
Исследователи уже с нетерпением ждут следующих шагов и стремятся отладить технологию. « Мы дорабатываем конструкцию nMOF и поставку PAMP, готовясь к испытаниям на людях », – заявил Линь. « Мы действительно работаем над увеличением лучшего состава, чтобы мы могли провести его в клинических испытаниях, надеюсь, в ближайшие два-три года или даже раньше ».
Исследователи признают междисциплинарный характер сотрудничества Калифорнийского университета в Чикаго и медицинского кампуса в Гайд-парке Чикагского медицинского университета за создание пространства, в котором биология рака и химия объединились для создания такого обнадеживающего потенциального лечения, а также поддержку, которую они получили от Ludwig Cancer Research в пути.
От концепции этого проекта и получения его финансирования до начала клинических испытаний, где мы можем протестировать технологию в клинических испытаниях и получить реальные данные пациентов, вся эта работа была проделана прямо здесь, в Калифорнийском университете в Чикаго . Мы действительно переходим от открытия чего-то в лаборатории к его тестированию у постели больного .
Ральф Вайксельбаум, доктор медицины, соавтор исследования и Даниэль К. Людвиг, заслуженный профессор радиационной и клеточной онкологии, Медицинский центр Чикагского университета
Исследование под названием «Наноразмерные металлоорганические каркасы для вакцинации против рака in situ с использованием рентгеновского излучения» финансировалось Национальным институтом рака (U01-CA198989 и 1R01CA253655), Министерством обороны (PC170934P2), Чикагским университетом. Комплексный онкологический центр медицины (NIH CCSG: P30 CA014599) и Институт исследования метастазов Людвига
Дополнительными авторами исследования являются Кайюань Ни, Гуансю Лан, Нининг Го, Август Калберт, Таокун Ло и Тонг Ву из Чикагского университета.
Ссылка на журнал:
Ni, K., и др. . (2020) Наноразмерные металлоорганические основы для вакцинации против рака in situ, активируемой рентгеновскими лучами. Достижения науки . doi.org/10.1126/sciadv.abb5223.
Источник: https://www.uchicagomedicine.org/[19459008visible
 Диэнай
Диэнай