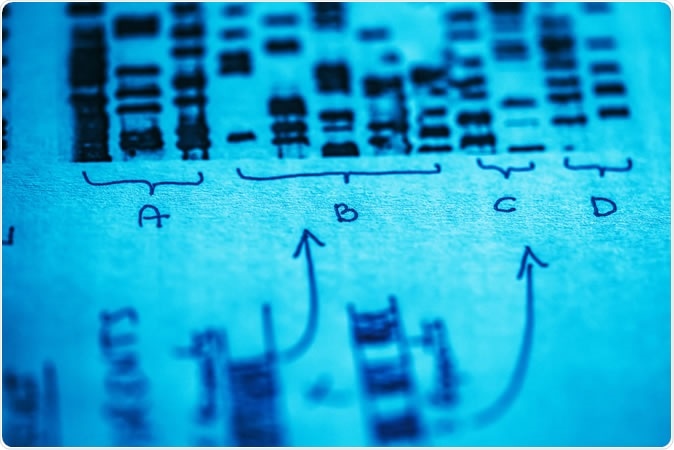
Новое исследование, опубликованное в журнале Nature Communications показывает, что может быть возможно обратить вспять мутации генов, которые вызывают нарушения головного мозга, с использованием очень точно нацеленной техники редактирования эпигенома. Этот тип редактирования генов не изменяет саму последовательность гена ДНК, а направлен только на исправление изменений эпигенома. Состояние, которое было исправлено в исследовании, называется синдромом WAGR и связано с ожирением и умственными нарушениями у людей.
Изображение предоставлено: isak55 / Shutterstock
Нейрональные гены и развитие мозга
Многие нарушения развития мозга, в том числе расстройства аутистического спектра, которые проявляются в раннем детском возрасте или позже, являются результатом плохо сформированного коммуникационного пути между двумя полушариями мозга. Это, в свою очередь, связано с отказами механизма, связанного с хроматином, один из которых был исправлен в текущем исследовании.
Ген, который они исправили, называется C11orf46 и имеет решающее значение для контроля развития мозга. Он отвечает за выработку ядерного белка, который регулирует некоторые важные белки, которые способны направлять новообразованные длинные нервные волокна, растущие из развивающихся нервных клеток, в правильной ориентации. Эти чувствительные к направлению белки помогают волокнам белого вещества связываться вместе и формировать большой нервный ствол, который пересекает пространство между двумя полушариями. Это мозолистое тело, и когда оно неправильно сформировано, человек может стать инвалидом, развить аутизм или другое нарушение развития мозга. Дефекты в гене C11orf46 связаны с гипоплазией или плохим развитием мозолистого тела.
Здоровый мозг человека (слева) и мозг с синдромом WAGR, при котором мозолистое тело тоньше и имеет неправильную форму. Изображение предоставлено компанией Nature Communications
Когда этот ген был сбит с ног, проекции аксонов из одного полушария головного мозга в другое были нарушены. В то же время множественные гены, которые кодируют определенные существенные события, которые регулируют развитие нервных волокон, сверхэкспрессируются в этих клетках. Одним из них является ген Semaphorin 6a. Это нормализуется посредством эпигенетического редактирования в настоящем исследовании, что приводит к нормализации экспрессии гена и восстановлению нормальной связности в мозолистом теле.
Короче говоря, нервные волокна, связывающиеся между полушариями, отвечают на специфическое ремоделирование нейронного генетического вещества в определенных местах.
Синдром WAGR
Также называемый синдромом делеции хромосомы IIp13, синдром WAGR возникает, когда часть или весь ген, который формирует C11orf46, в одноименной области хромосомы, случайно исключается во время деления клетки. Потеря этого белкового продукта вызывает тяжелую нетрудоспособность, характерную для этого синдрома.
В исследовании использовался инструмент для изменения генов, называемый РНК с короткой шпилькой, чтобы уменьшить выработку белка в мозге мыши. В результате нервные волокна в развивающемся мозге не могли сформироваться в пучок мозолистого тела белого вещества, что привело к состоянию, очень напоминающему WAGR. Это подтверждает, что C11orf46 важен в соединении белого вещества, опосредуя этот процесс через гены, которые помогают соединять аксоны по обе стороны мозолистого тела.
Механизм нарушения связи при дисфункции C11orf46
Что происходит, когда продукт гена C11orf46 субнормален? Мозг мыши в этой ситуации сверхэкспрессирует другой ген, который отвечает за выработку семафорина 6a, белка, чувствительного к направлению, а также многих других белков, таких как Doublecortin-like kinase 1 (Dclk1) и SLIT-ROBO Rho GTPase активирующий белок 3 ( Srgap3). Короче говоря, это регулятор транскрипции во время фазы развития мозга.
C11orf46 взаимодействует с другим регионом, называемым KMT-RC. Мутации в C11orf46 предотвращают эту связь с этим комплексом и препятствуют правильному развитию мозга. Исследователи проверили свою теорию, что аффинность связывания C11orf46 с этим комплексом может быть использована для изменения паттерна экспрессии генов.
Редактирование эпигенома
Одним из способов является редактирование эпигенома с использованием редактирования гена CRISPR, но это может быть неэффективным. Поэтому исследователи адаптировали эту систему для изменения регуляторной области для семафорина 6а – эпигеномного изменения.
В результате они обнаружили, что низкие уровни C11orf46 теперь способны связываться с областью гена Semaphorin 6a и подавлять его, снижая его экспрессию. Это восстановило способность нервных волокон связываться так же, как в нормальном мозге.
Заключение
Этот вид оригинальной терапии может помочь продвинуть технологию редактирования эпигенома, чтобы разработать новые методы лечения, которые могут реконструировать нервные связи мозга. Фактически, это может в один прекрасный день предотвратить развитие мозга как нарушения развития, считает исследователь Ацуши Камия. В заключении доклада говорится, что такие исследования могут «проложить путь для нового лечения психических состояний нервного развития в раннем возрасте».
Ссылка на журнал:
Эпигенетическое редактирование промотора Sema6a in vivo устраняет транскаллозальную дисконнективность, вызванную геном риска C11orf46 / Arl14ep. Кирилл Дж. Питер, Ацуши Сайто, Юто Хасегава, Юя Танака, Мохика Нагпал, Габриэль Перес, Эмили Алвей, Серхио Эспесо-Гил, Тарик Файяд, Чана Ратнер, Аслихан Динсер, Ахла Гупта, Лакшми Деви, Джон Дж. Паппо, Франс Лалонде, Джон А. Бутман, Джоан С. Хан, Шахрам Акбарян и Ацуши Камия. Nature Communications, том 10, номер статьи: 4112 (2019). https://doi.org/10.1038/s41467-019-12013-y. https://www.nature.com/articles/s41467-019-12013-y#Sec7
 Диэнай
Диэнай